As funções inorgânicas englobam os ácidos, as bases, os sais e os óxidos. Além disso, dentro das funções inorgânicas, encontramos o principal óxido, sem o qual não sobreviveríamos: a água.
Funções Inorgânicas: Ácidos
Os ácidos se enquadram em funções inorgânicas. Eles são moléculas que na presença de água liberam o cátion H+ (próton), e que aceita receber um par de elétrons.
Os compostos ácidos são sempre substâncias que contém hidrogênio (H) em suas moléculas. Em
nosso organismo ou em soluções (em água por exemplo), eles liberam esse H sem um elétron, ou seja, liberam um cátion de hidrogênio H+ (íon positivo, em que o sinal de + indica a perda de elétrons). Portanto, essa é a característica mais marcante dos ácidos.
Veja as representações de alguns ácidos que estão presentes constantemente em nossas
vidas:
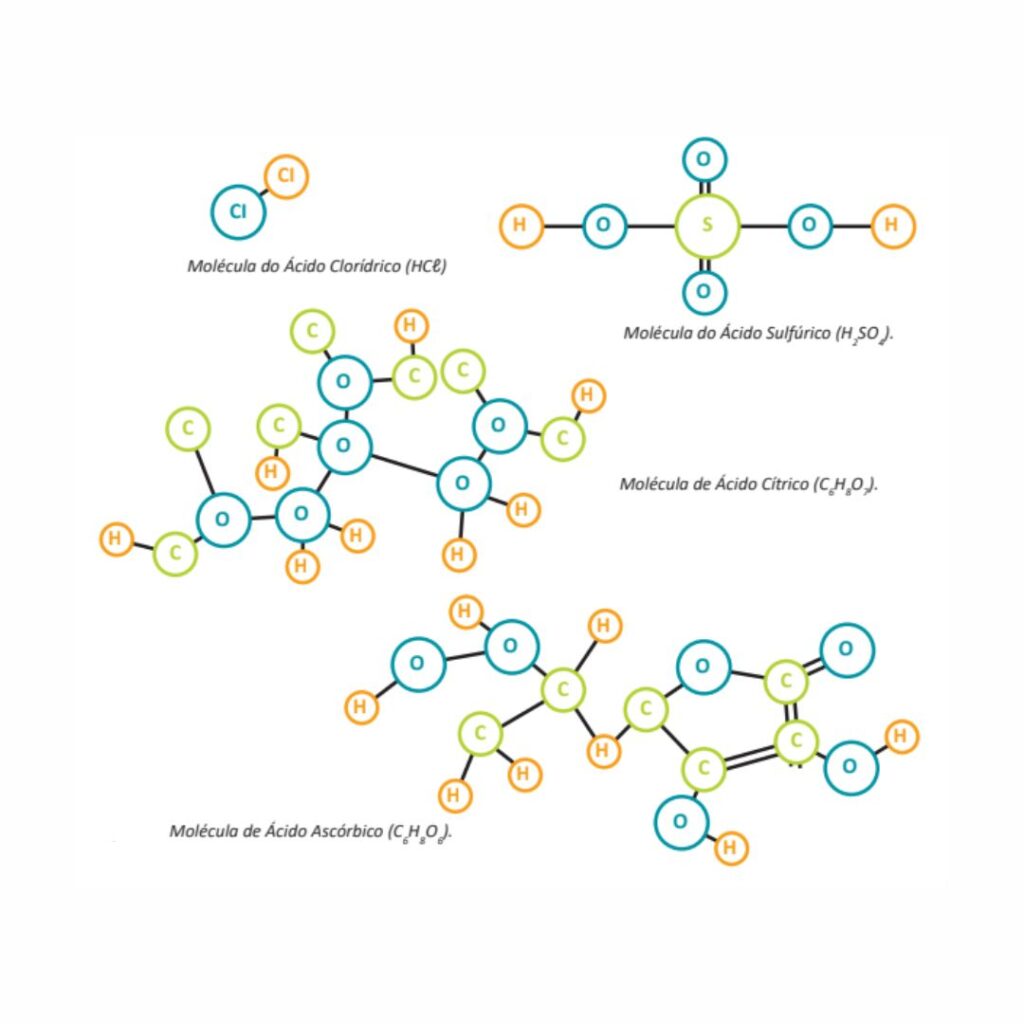
- HCl – Ácido Clorídrico: conhecido como suco gástrico (ácido fabricado pelo corpo humano para digerir os alimentos no estômago), o mesmo ácido muriático usado na limpeza pesada de pisos. O Ácido Clorídrico é um exemplo de ácidos inorgânicos hidrácidos, que são os ácidos que não contêm o oxigênio em sua molécula.
- H2SO4 – Ácido Sulfúrico: as baterias de carro usam ácido sulfúrico e podemos considerar ele como um dos ácidos mais prejudiciais, pois é extremamente corrosivo. Esse ácido é encontrado nas chuvas ácidas. O Ácido Sulfúrico é um exemplo de ácidos inorgânicos oxiácidos, que são os ácidos que contêm o oxigênio em suas moléculas.
- C6H8O7 – Ácido Cítrico: esse é o nome popular usado, pois seu nome oficial é complexo de escrever e de ler. O Ácido Cítrico é um ácido orgânico presente nas frutas ácidas.
- C6H8O6 – Ácido Ascórbico: a famosa Vitamina C. Ele também é um ácido orgânico, que é encontrado nos alimentos ácidos naturais e é excelente para manter a saúde.
Funções Inorgânicas: Bases
As bases são outras funções inorgânicas, elas são moléculas que na presença de água liberam o ânion OH- (hidroxila), e que oferece um par de elétrons.
Nesse sentido, os compostos básicos ou alcalinos estão em diversas vitaminas que são necessárias para nosso corpo. Ademais, eles são encontrados também em diversos produtos, como alguns remédios e produtos de limpeza.
Esses compostos básicos são substâncias que se caracterizam pela existência do ânion hidroxila, OH- (que é um íon negativo, onde o sinal – signifia que ganhou elétrons), sendo assim fácil de identificar a presença desse íon na molécula, que é uma característica marcante das bases.
Vejamos as representações de algumas bases que estão presentes em diversas situações das nossas vidas:
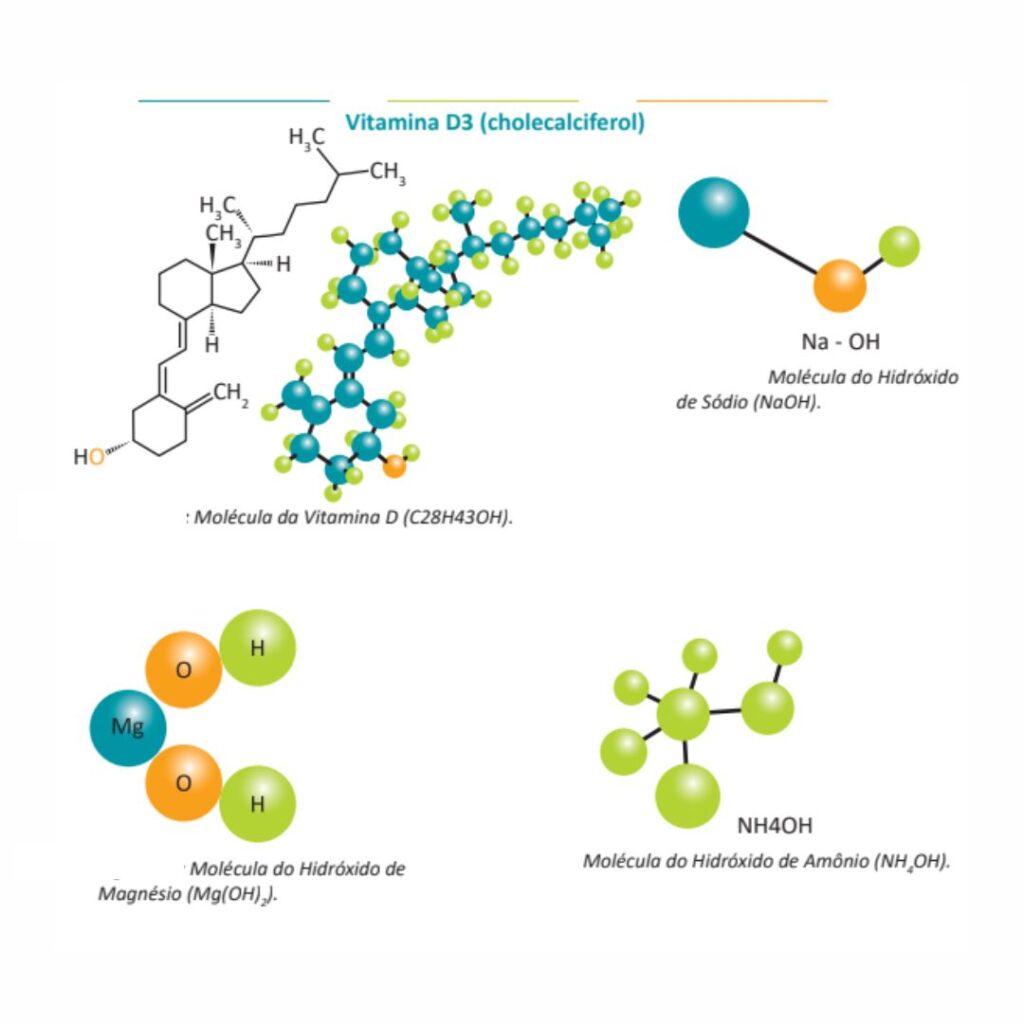
- C28H43OH – Vitamina D: é uma base orgânica com um nome meio complexo. Ela ajuda a absorver o cálcio dos alimentos, contribuindo com a calcificação dos ossos. Nesse sentido, a vitamina D é uma excelente protetora contra o câncer de mama e de próstata.
- NaOH – Hidróxido de Sódio: comumente chamada de soda cáustica, usada na fabricação de sabão. O Hidróxido de Sódio é usado também como antiácido estomacal quando tomamos bicarbonato de sódio, que, na presença, de água libera o hidróxido de sódio que vai reagir com o ácido estomacal.
- Mg(OH)2 – Hidróxido de Magnésio: é o leite de magnésio usado como antiácido para combater as queimações no estômago (acidez estomacal).
- NH4OH – Hidróxido de Amônio: conhecido como amoníaco, usado para descolorir o cabelo ou os pelos do corpo.
Funções Inorgânicas: Sais
Em primeiro lugar, os sais são funções inorgânicas que correspondem a compostos iônicos que em solução aquosa liberam ao menos um cátion diferente do H+, e ao menos um ânion diferente de OH-.
Nesse sentido, uma das formas de produção dos sais é pela reação entre ácidos e bases (reação de neutralização) e a outra forma é a extração da natureza.
Dessa maneira, ao dissolver os sais em água, eles liberam ao menos um cátion diferente do íon H+ e liberam também ao menos um ânion diferente do íon OH-.
Os sais em nosso organismo
Os sais minerais são de grande importância para o bom funcionamento do nosso organismo. Na couve crua encontramos por exemplo: o cálcio, o fósforo e o ferro.
- Cálcio – atua na coagulação do sangue, contração muscular, bom funcionamento dos nervos e constitui os ossos e dentes;
- Fósforo – é responsável por transferir energia no interior das células, e é um dos constituintes dos ossos, dos dentes, do DNA e do RNA;
- Ferro – é um dos constituintes da hemoglobina, as células vermelhas do sangue. Ele é importante para a respiração celular.
Formação dos sais
A formação dos sais acontece pela reação entre os ácidos e as bases (reagentes), podemos verificar os sais formados com alguns dos exemplos de ácidos e bases vistos anteriormente. Além disso, é bom saber que essa reação sempre forma um sal e água (produto).
Nesse sentido, é bom também relembrar que as reações químicas acontecem sempre entre os reagentes que reagem e formam os produtos.
Reações com os ácidos que não possuem o oxigênio em suas moléculas (ácidos hidrácidos):

Essa é a reação de uma das funções inorgânicas que acontece quando tomamos o bicarbonato de sódio dissolvido em água (NaOH) para acabar com a azia. Nela ocorre a formação do sal NaCl – Cloreto de Sódio – em nosso estômago.
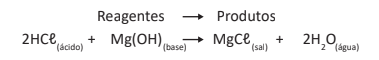
Essa reação acima ocorre quando tomamos o leite de magnésio, formando no estômago o sal MgCl2 – Cloreto de Magnésio – e duas moléculas de água. Além disso, vale destacar que o cloreto de magnésio regulariza a pressão arterial, ajuda a melhorar o aprendizado e a memória, minimiza o estresse, e tem outras utilidades benéficas para o nosso corpo.
Reações com os ácidos que possuem o oxigênio em suas moléculas (ácidos oxiácidos):

Essa é uma reação entre o ácido sulfúrico (H2SO4) e o hidróxido de sódio (2NaOH) que tem como produto o Na2 SO4 – Sulfato de Sódio – e duas moléculas de água (2H2O). Ademais, o sulfato de sódio é um sal branco usado na fabricação de celulose nas indústrias de papel. Também usam ele para remover as bolhas de ar na fabricação de vidro, no tangimento de tecidos e na fabricação de sabão.

Nessa reação temos o ácido sulfúrico (H2SO4) reagindo com o hidróxido de magnésio (Mg(OH)2), tendo como produto o MgSO4 – Sulfato de Magnésio – e duas moléculas de água (2H2 O). Em suma, o sulfato de magnésio, mais conhecido como sal amargo, possui ação laxante (solta o intestino) e podemos usá-los em massagens e banhos relaxantes.
Funções Inorgânicas: Óxidos
Os óxidos também são funções inorgânicas, eles são compostos binários (apenas dois elementos) em que um deles é o oxigênio. Nos óxidos o composto que tem maior afinidade por elétrons é o oxigênio. Nesse sentido, a maioria dos elementos químicos forma óxidos com o oxigênio.
O óxido mais importante, comum e consumido por todas as pessoas é o óxido de hidrogênio, conhecido como água (H2O). Da mesma forma, outro dos óxidos conhecidos é o óxido de ferro ou óxido férrico (Fe2O3), que é a ferrugem que encontramos em peças de ferro (em alguns portões antigos e sem pintura conseguimos ver claramente o óxido de ferro).
